肿瘤免疫治疗进展中的老将和新秀
- 头条资讯
- 2016-05-09
点击上方“转化医学网”订阅我们!
干货 | 靠谱 | 实用

近年来,肿瘤的免疫治疗则因其对于常规疗法无效的晚期肿瘤具有显著疗效而受到极大关注,并于2013年被Science评为年度十大科技突破之首,为转移性晚期肿瘤治疗带来新的希望。肿瘤免疫学治疗的目的是激发或调动机体的免疫系统,增强肿瘤微环境抗肿瘤免疫力,从而控制和杀伤肿瘤细胞。肿瘤免疫学治疗的方法种类繁多,已与现代生物高科技技术结合,发展成为继手术、化疗和放疗之后的第四种肿瘤治疗模式-肿瘤生物学治疗方法。目前肿瘤的免疫疗法主要包括治疗性疫苗、细胞因子、免疫调节剂、免疫抑制剂和T细胞过继治疗。下面我们就来谈谈在免疫治疗药物发展中起着举足轻重作用的老将和新秀们。
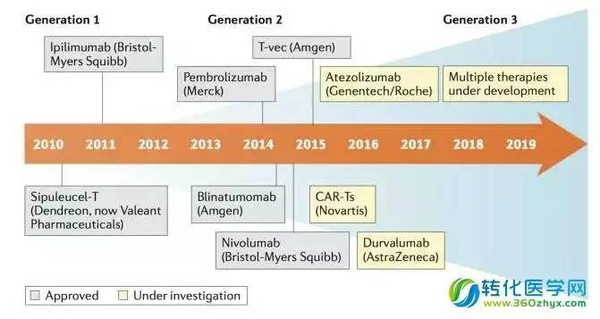
图一 肿瘤免疫治疗药物的发展史
1
CTLA-4
细胞毒T淋巴细胞抗原4(CTLA-4)又名CD152,是由CTLA-4基因编码的一种跨膜蛋白质,表达于活化的CD4+和CD8+T细胞。CTLA-4与其配体B7分子结合后产生抑制性信号,抑制T细胞激活,使肿瘤细胞免受T淋巴细胞攻击。因此阻断CTLA-4的免疫效应可刺激免疫细胞大量增殖,从而诱导或增强抗肿瘤免疫反应。
CTLA-4为许多疾病包括肿瘤的免疫治疗提供了新的方法。抗CTLA-4抗体用于肿瘤的免疫治疗,是目前肿瘤靶向免疫治疗的热点。目前两种靶向CTLA-4的抗体Ipilimumab和Tremelimumab均已进入Ⅲ期临床试验,已广泛用于治疗黑色素瘤、肾癌、前列腺癌、肺癌等。Ⅰ/Ⅱ期临床研究结果显示两种抗体无论是抗体单药还是联合IL-2,gp100疫苗或化疗均显示安全有效。抗CTLA-4抗体如Ipilimumab和Tremelimumab,尤其是Ipilimumab,在肺癌的Ⅰ-Ⅱ期临床研究中均显示了较好的疗效,开启了肿瘤治疗的新时代。
2
PD-1
PD-1免疫疗法是当前肿瘤界最热的新一类抗癌免疫疗法,具有治疗多种类型肿瘤的潜力。其不同于以往肿瘤靶向治疗药物,PD-1抑制剂靶向肿瘤免疫而非肿瘤细胞本身。那么,神奇的PD-1抑制剂是如何抗击肿瘤的呢?
PD-1作为负性调控点,在体内与特异性配体(PD-L1、PD-L2)结合起作用,下调抗原刺激的淋巴细胞增殖、细胞因子的产生和生存蛋白的表达,最终导致淋巴细胞“耗尽”以及诱导免疫耐受的产生,同时上调免疫抑制细胞因子白细胞介素10的分泌,最终导致免疫逃逸,抑制T细胞的抗肿瘤作用。下面我们将盘点当下最耀眼的PD1/PDL。PD-1抑制剂通过特异性的结合PD-1,阻断PD-1及其配体介导的信号通路,上调T细胞对肿瘤细胞的免疫应答。
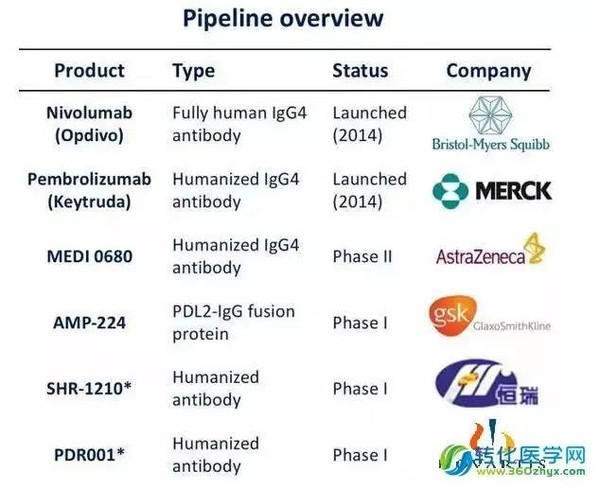
图二 目前处于各个阶段的PD-1抗体
Opdivo(Nivolumab,也称BMS-936559)是抗PD-1的全人源IgG4单克隆抗体。Opdivo于2014年7月获得日本PMDA批准用于晚期黑色素瘤的治疗,成为全球首个获批的抗PD-1单抗,随后又获批了非小细胞肺癌和肾细胞癌的适应症。 Merck的Keytruda是抗PD-1的人源化IgG4单克隆抗体。与2014年9月获得FDA 批准治疗恶性黑色素瘤。随后又被批准治疗非小细胞肺癌。在国内的临床试验方面,Opdivo已于2015年7月获CDE批准进行临床试验,用于晚期或转移性的非小细胞肺癌,晚期或复发性实体瘤治疗。而Keytruda在今年1月27日也获得了CDE的临床试验批件,PD-1抑制剂市场的两大巨头在世界主要癌症市场的竞争已经全面展开。
尽管目前国内暂无抗PD-1单克隆抗体获批生产,但竞争也相当激烈。上个月,领头的君实生物、恒瑞医药各自的PD-1抗体I期临床均启动。紧随其后的两家公司分别为百济神州和嘉和生物,两者的PD-1抗体临床试验申请分别于去年11月及今年2月获受理。鉴于免疫检查点抑制剂展现出的广阔市场前景,国内越来越的企业开始涉足这一领域。4月25日,誉衡药业发布公告称,公司与药明康德共同研发的抗PD-1全人创新抗体药(GLS-010注射液)临床研究申请获得受理(受理号:CXSL1600045黑)。
3
PD-L1
同样, PD-L1药物也值得关注。默克(Merck KGaA)和辉瑞(Pfizer)合作开发的抗PD-L1免疫疗法avelumab,FDA已授予avelumab治疗既往已接受至少一种化疗方案的转移性Merkel细胞癌(merkel cell carcinoma,MCC)患者的突破性药物资格。同时FDA还授予avelumab孤儿药地位和快车道地位。此次收获突破性药物资格,标志着avelumab临床开发的第三个重要里程碑,有望加速avelumab治疗转移性MCC的临床开发进程。
目前在PD-L1领域还需关注的公司包括罗氏、阿斯利康等。罗氏宣布其开发的PD-L1药物atezolizumab在一项治疗非细小性细胞肺癌的临床二期研究中取得了重大成功。生物技术公司Syndax宣布与罗氏旗下的Genentech公司签订了合作协议,双方将合作开发Syndax公司新型肿瘤药物entinostat与atezolizumab在多种肿瘤类型上的联合治疗效果。
另一个需要关注的产品是阿斯利康(AZ)的durvalumab((MEDI4736))。为了抢占肿瘤免疫治疗市场,AZ将这款产品“绑定”了Peregrine、Mirati等公司,开展联合疗法。
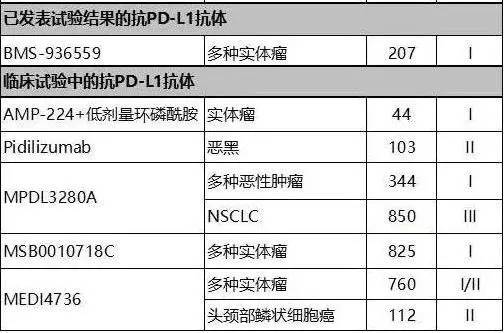
图三 临床各阶段中的PD-L1抗体
4
CAR-T细胞疗法
2013年,科学家们宣布使用一种新型的免疫细胞疗法成功治愈晚期急性淋巴细胞白血病,给全世界癌症病人带来了新的曙光。这种利用嵌合型抗原受体转基因T细胞(Chimeric Antigen Receptor T-Cell, CaR-T)免疫治疗方法,可以特异性地识别肿瘤相关抗原,最终达到治愈肿瘤的目的。小女孩艾米丽-怀特黑德(Emily Whitehead)的故事激励着无数科研工作者投身到Car T研究中。接受治疗后两年,艾米丽身体健康,能像其他正常孩子一样享受生活。
以CAR-T细胞技术为主的过继性免疫治疗(被动免疫),包括LAK细胞、CIK细胞、CTL细胞、TIL细胞等。CD19是一个理想的抗原,因为它在分化的B细胞上广泛表达,但不在造血干细胞或其它重要细胞类型中表达。CD19抗原特异性CAR-T 细胞用于治疗B细胞白血病和淋巴瘤临床试验中,显示出持续的疾病缓解效果。由于CAR-T/TCR-T技术的优越表现,以及广阔的应用前景,从而使其进入了当前激烈的制药行业竞技舞台中与传统的制药业一较高低。
新晋制药公司Kite Pharma宣布联手行业巨头安进,共同研发其CAR-T肿瘤免疫疗法。其主要候选药物KTE-C19近日闪电收获FDA突破性疗法认证,预计明年会提交上市申请。与此同时,Kite正准备开展KTE-C19针对晚期/非晚期急性淋巴细胞白血病儿童的第四个关键临床试验。
美国制药巨头辉瑞(Pfizer)近日与法国药企施维雅(Servier)抢购了由法国生物技术公司Cellectis开发的一款针对血液癌症极具治疗潜力的CAR-T细胞疗法UCART19。该CAR-T细胞疗法即将进入I期临床试验,用于慢性淋巴细胞白血病(CLL)和急性淋巴细胞白血病(ALL)的潜在治疗。另一方面,辉瑞与施维雅也达成了一项独家全球授权及合作协议,双方将合作开发及商业化UCART19。
5
CD73
日前,Cell旗下《Trends in Cancer》发表了一篇题为“Anti-CD73 in Cancer Immunotherapy: Awakening New Opportunities”的综述。这一综述讨论了CD73与肿瘤发生、发展以及扩散之间的关系,强调了这一分子作为药物靶标的潜在价值,并表示CD73有望成为个性化癌症治疗中的新生物标志物。
尽管CTLA-4、PD-1和PD-L1抑制已经在临床中成功应用,但科学家们也在积极研究其它的检查点通路。在这些通路中,ecto-5′-nucleotidase (CD73)在驱动癌症免疫逃逸中发挥了关键的作用。最新的证据表明,调整嘌呤代谢是非常关键的一步,尤其是增加ecto-5′-nucleotidase(CD73)的表达。这种降解酶能够使AMP脱去磷酸,从而会导致肿瘤微环境中免疫抑制和pro-angiogenic adenosine halo的产生,促进癌症的发生和发展。因此,可能成为发展新型抗癌免疫疗法极具潜力的靶点。
临床前研究表明,靶向CD73能够产生良好的抗肿瘤作用,且将CD73阻断治疗与其它免疫分子调节剂联合(如CTLA-4抗体、PD-1抗体)是一种极具吸引力的选择。作者们表示,尽管还有很长的路要走,但是通过CD73抗体的发展,抗CD73治疗有望成为抗癌领域的新型生物疗法。
联合用药
对于晚期肿瘤患者,由于肿瘤负荷大,体内抗肿瘤微环境的改变以及免疫耐受的产生(Treg细胞)等,机体不能有效地启动免疫应答反应,从而导致对单一免疫治疗的疗效不敏感。基于此,有学者提出,单一免疫治疗或许对低肿瘤负荷如早期或化疗后的患者更为有效,而联合免疫治疗或许能使晚期肿瘤患者获益。目前,很多临床试验者正试图将这类药物与其他的癌症疗法(如放疗、化疗、溶瘤病毒、细胞疗法等)组合在一起,期望找到更有效的联合疗法。
最初进行的一例联合疗法试验是将Ipilimumab和Nivolumanb这两种检查点抑制剂组合在一起。试验结果发现,这种联合疗法对58%的晚期黑色素瘤患者有效,而Ipilimumab单独使用只对19%的病人有效。虽然,这两种检查点抑制剂靶点(CTLA-4和PD-1)都会抑制T细胞的激活,但是它们分别作用于T细胞激活过程中的不同阶段。可以想见,同时阻断CTLA-4和PD-1的功能可以更有效的激活T细胞,故而对肿瘤杀伤力更大。
“这不是盲目地堆砌药物,”纽约纪念斯隆-凯特琳癌症中心(Memorial Sloan Kettering Cancer Center) 的肿瘤科医生Jedd Wolchok说,“而是在理解药物机理的同时,找出在什么时候需要什么样的药物。”
2015年9月30日,美国食品药品监督管理局(以下简称FDA)加速批准PD-1抑制剂(Nivolumab)联合CTLA-4抑制剂Ipilimumab治疗BRAF V600野生型、不可切除的或转移性黑色素瘤。目前也有多项研究针对肿瘤的其他联合免疫治疗已经开展并取得了初步疗效。
图四 正在进行的针对肿瘤联合免疫治疗
临床前及临床试验结果均表明,联合治疗可能是肿瘤免疫治疗更有效的治疗方式。免疫治疗在肺癌发展迅速,已有许多临床试验在进行中。虽然仍有许多问题尚待进一步解决,但我们相信免疫治疗在癌症综合治疗中的良好前景。随着肿瘤免疫治疗的技术越来越发展,越来越多的靶点和检查点被发现。肿瘤免疫药物将会如雨后春笋般冒出来,让我们拭目以待……
— END—
点击" 阅读原文"下载转折点APP!
一般声明:本站文章来源于网络。
下一篇:江淮车系3款新秀银川亮相